COME AGISCE
Quando le cellule tumorali sono sottoposte a temperature elevate (43-44 °C) subiscono un danno irreversibile (strettamente dipendente dalla temperatura raggiunta e dal tempo di applicazione) legato ad una riduzione dell’efficacia dei sistemi di riparazione normalmente presenti nella cellula sana.
A 43-44°C la maggior parte delle cellule tumorali tende a subire un danno che gradualmente ne provocherà la morte mediante un meccanismo noto come apoptosi: questa è la base fisiologica dell’efficacia terapeutica dell’IPERTERMIA ONCOLOGICA.
La maggior sensibilità della cellula tumorale al calore dipende in parte dalle proprie caratteristiche genetiche e in parte dal microambiente in cui la cellula tumorale viene a trovarsi.
L’IPERTERMIA ONCOLOGICA attiva nelle cellule tumorali geni che a loro volta codificano per proteine, note con il nome di caspasi, in grado di attivare il meccanismo di morte cellulare per apoptosi (definita anche “suicidio” cellulare).
È stato ampiamente dimostrato, dapprima su linee cellulari tumorali coltivate in vitro, successivamente nell’animale e quindi nell’uomo, come l’uso di IPERTERMIA ONCOLOGICA provochi l’induzione di apoptosi in un elevato numero di cellule tumorali.
Tale fenomeno può essere incrementato dalla contemporanea somministrazione di farmaci chemioterapici e/o immunoterapici e dalla radioterapia che possono pertanto essere vantaggiosamente associati con un incremento dell’efficacia grazie ad una sinergia di distruzione delle cellule tumorali.
PRINCIPALI EFFETTI
- Induce direttamente la morte delle cellule tumorali innescando, mediante l’incremento di temperatura, l’attivazione il fenomeno di apoptosi.
- Sensibilizza le cellule all’azione dei farmaci (chemioterapia, immunoterapia, anticorpi monoclonali, terapie anti-ormonali, ecc.).
- Potenzia l’efficacia della radioterapia anche a livello dei tessuti poco ossigenati e poco vascolarizzati.
- Attiva le difese immunitarie dell’organismo (in particolare nell’IPERTERMIA TOTAL-BODY) nei confronti della progressione e disseminazione del tumore.
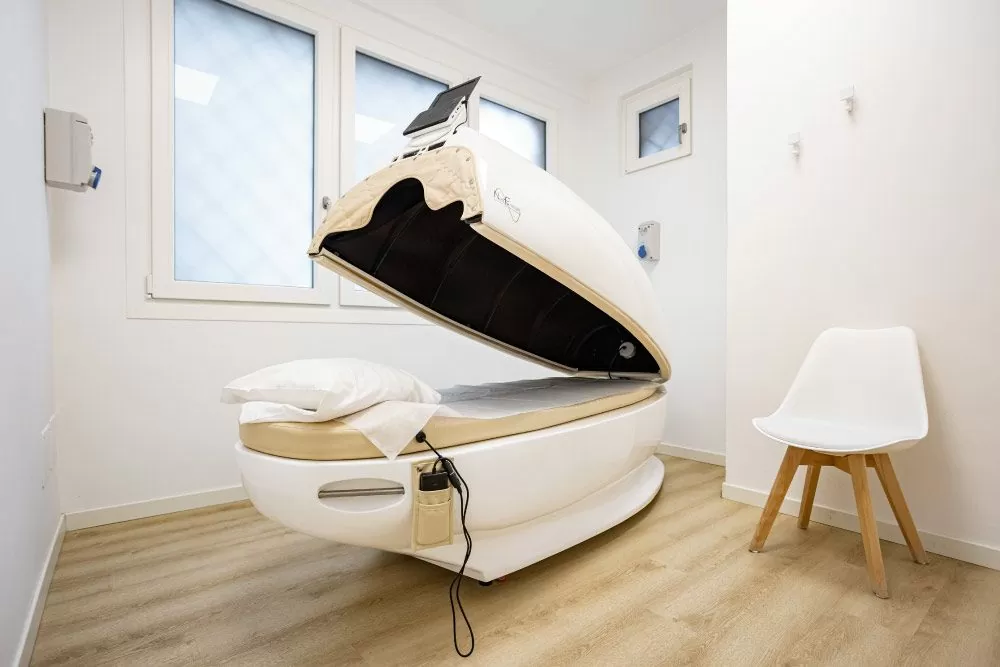
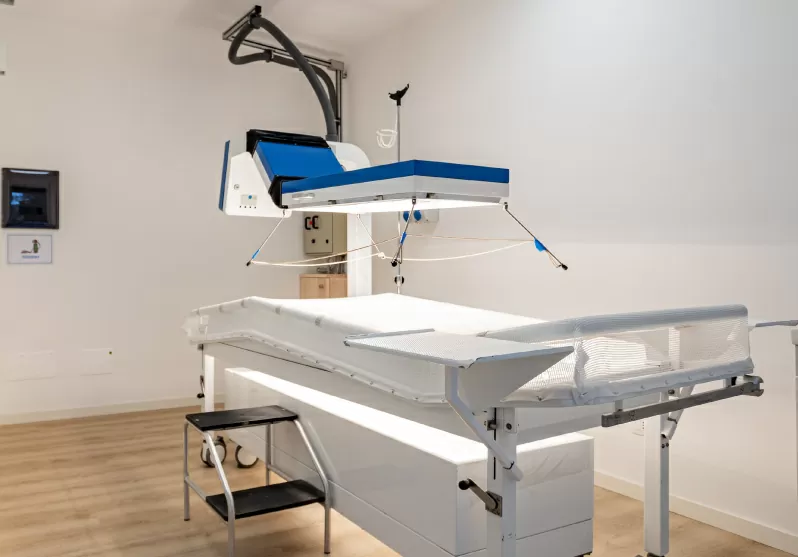
Dal punto di vista tecnico l’IPERTERMIA ONCOLOGICA può essere indotta con diverse metodiche. Il nostro Centro dispone di tutte le tipologie di apparecchiature ad oggi disponibili nella pratica clinica:
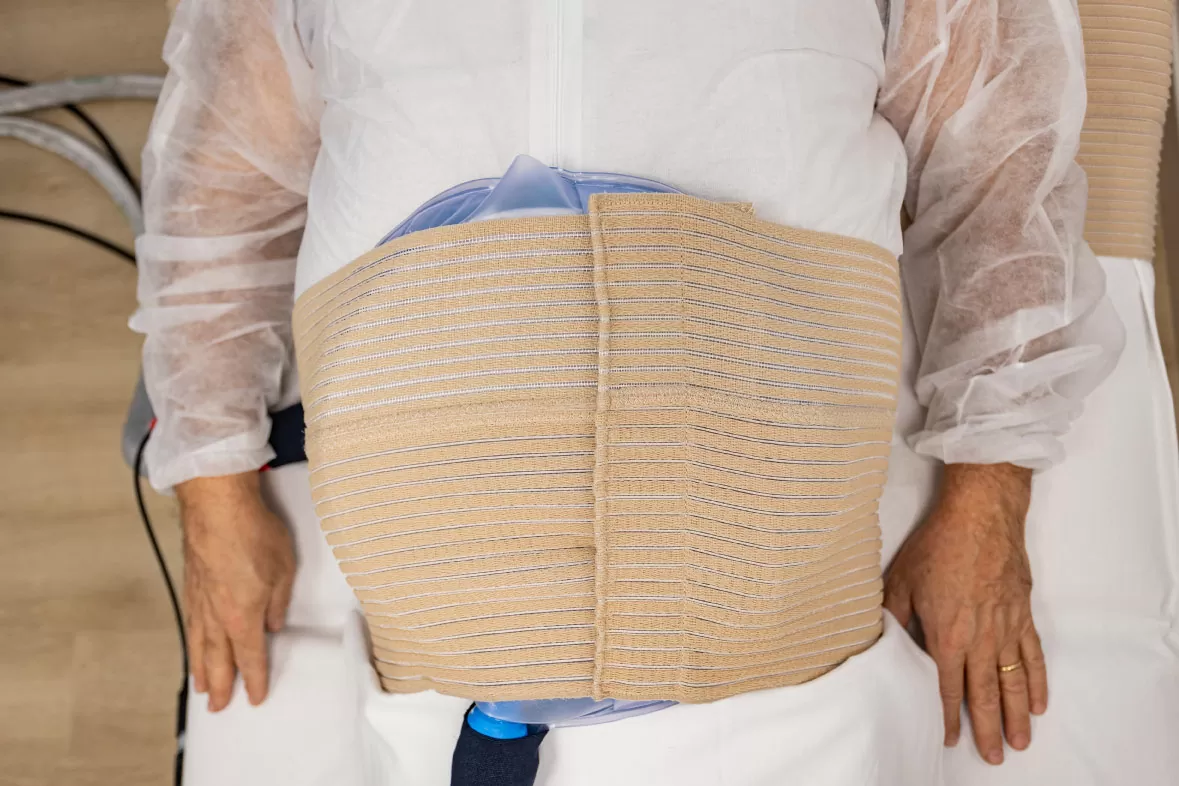
- IPERTERMIA A RADIOFREQUENZE (13.56 MHz) in grado di ottenere un riscaldamento ottimale dei tessuti profondi. Viene utilizzata per il trattamento localizzato di tutte le forme tumorali solide, primitive o metastatiche.
- IPERTERMIA TOTAL-BODY a raggi infrarossi lunghi , trova impiego nei trattamenti di prevenzione delle recidive, nelle forme disseminate, nei trattamenti di regolazione immunitaria per patologie auto-immuni o infezioni croniche.
IPERTERMIAONCOLOGICA E RADIOTERAPIA
L’utilizzo concomitante di IPERTERMIA ONCOLOGICA e radioterapia potenzia l’effetto della radiazioni ionizzanti con meccanismo:
- Superaddittivo, cioè con un sommarsi degli effetti maggiore di quanto atteso dall’applicazione indipendente dei due trattamenti. Tale potenziamento è massimo se i due trattamenti vengono somministrati entro un breve intervallo di tempo.
- Complementare in quanto le cellule radioresistenti sono normalmente sensibili alla terapia con il calore.
Numerosi trials clinici hanno documentato un incremento di risposte complete di circa 1.5/2 volte nel trattamento associato delle recidive locali di carcinoma mammario, delle metastasi linfonodali di neoplasie del distretto testa-collo e delle metastasi cutanee, sottocutanee e linfonodali di melanoma, nei tumori della cervice uterina e nei tumori cerebrali (incluso il glioblastoma), nelle metastasi scheletriche.
Promettenti sono anche i risultati ottenuti dall’associazione di IPERTERMIA ONCOLOGICA e radioterapia nell’impiego neoadiuvante (cioè prima dell’intervento chirurgico, con l’obiettivo di favorirne la radicalità) nei tumori del retto e della mammella.

IPERTERMIA ONCOLOGICA E CHEMIOTERAPIA
Quando le cellule sono esposte ai farmaci in condizioni di IPERTERMIA esse reagiscono molto spesso in maniera diversa rispetto a quanto avviene a 37°C.
I farmaci il cui effetto è soprattutto di tipo chimico (non coinvolge cioè sistemi enzimatici) sono generalmente più efficaci alle elevate temperature. I processi di alchilazione del DNA o la conversione da una forma inattiva a una forma attiva avvengono più facilmente alle alte temperature. Anche il pH cellulare può influenzare l’attività dei farmaci. Su tali osservazioni si basano i protocolli di associazione tra IPERTERMIA ONCOLOGICA e chemioterapia sistemica.
Tutti questi elementi portano alla conclusione che, per combattere efficacemente i tumori tutte le terapie in grado di provocare apoptosi devono essere utilizzate nell’intento di distruggere il maggior numero possibile di cellule tumorali, sostenendo nel contempo la funzione del sistema immunitario. Particolarmente efficaci risultano infatti le combinazioni di IPERTERMIA ONCOLOGICA ai trattamenti standard di chemioterapia, radioterapia e immunoterapia
PRINCIPALI INDICAZIONI AI TRATTAMENTI
Trattamento neoadiuvante
Trattamento neoadiuvante cioè in preparazione dell’intervento chirurgico (carcinoma mammario, tumori testa-collo, tumori colon-retto, carcinoma uterino, carcinoma della cervice, sarcomi, ecc.)
Trattamento adiuvante
trattamento adiuvante cioè di consolidamento dopo intervento chirurgico radicale o parziale
Trattamento in casi non operabili o con metastasi
trattamento in casi non operabili o con metastasi (vai alla pagina APPROFONDIMENTI)